关于蛋白质组学检测结果分析求助
1.蛋白质鉴定:可以利用一维电泳和二维电泳并结合Western等技术,利用蛋白质芯片和抗体芯片及免疫共沉淀等技术对蛋白质进行鉴定研究。2.翻译后修饰:很多mRNA表达产生的蛋白质要经历翻译后修饰如磷酸化,糖基化,酶原激活等。翻译后修饰是蛋白质调节功能的重要方式,因此对蛋白质翻译后修饰的研究对阐明蛋白质的功能具有重要作用。3.蛋白质功能确定:如分析酶活性和确定酶底物,细胞因子的生物分析/配基-受体结合分析。可以利用基因敲除和反义技术分析基因表达产物-蛋白质的功能。另外对蛋白质表达出来后在细胞内的定位研究也在一定程度上有助于蛋白质功能的了解。Clontech的荧光蛋白表达系统就是研究蛋白质在细胞内定位的一个很好的工具。4.对人类而言,蛋白质组学的研究最终要服务于人类的健康,主要指促进分子医学的发展。如寻找药物的靶分子。很多药物本身就是蛋白质,而很多药物的靶分子也是蛋白质。药物也可以干预蛋白质-蛋白质相互作用。在基础医学和疾病机理研究中,了解人不同发育、生长期和不同生理、病理条件下及不同细胞类型的基因表达的特点具有特别重要的意义。这些研究可能找到直接与特定生理或病理状态相关的分子,进一步为设计作用于特定靶分子的药物奠定基础。 不同发育、生长期和不同生理、病理条件下不同的细胞类型的基因表达是不一致的,因此对蛋白质表达的研究应该精确到细胞甚至亚细胞水平。可以利用免疫组织化学技术达到这个目的,但该技术的致命缺点是通量低。激光捕获显微切割LCM(Laser Capture Microdissection)技术可以精确地从组织切片中取出研究者感兴趣的细胞类型,因此LCM技术实际上是一种原位技术。取出的细胞用于蛋白质样品的制备,结合抗体芯片或二维电泳-质谱的技术路线,可以对蛋白质的表达进行原位的高通量的研究。很多研究采用匀浆组织制备蛋白质样品的技术路线,其研究结论值得怀疑,因为组织匀浆后不同细胞类型的蛋白质混杂在一起,最后得到的研究数据根本无法解释蛋白质在每类细胞中的表达情况。虽然培养细胞可以得到单一类型细胞,但体外培养的细胞很难模拟体内细胞的环境,因此这样研究得出的结论也很难用于解释在体实际情况。因此在研究中首先应该将不同细胞类型分离,分离出来的不同类型细胞可以用于基因表达研究,包括mRNA和蛋白质的表达。LCM技术获得的细胞可以用于蛋白质样品的制备。可以根据需要制备总蛋白,或膜蛋白,或**白等,也可以富集糖蛋白,或通过去除白蛋白来减少蛋白质类型的复杂程度。相关试剂盒均有厂商提供。 蛋白质样品中的不同类型的蛋白质可以通过二维电泳进行分离。二维电泳可以将不同种类的蛋白质按照等电点和分子量差异进行高分辨率的分离。成功的二维电泳可以将2000到3000种蛋白质进行分离。电泳后对胶进行高灵敏度的染色如银染和荧光染色。如果是比较两种样品之间蛋白质表达的异同,可以在同样条件下分别制备二者的蛋白质样品,然后在同样条件下进行二维电泳,染色后比较两块胶。也可以将二者的蛋白质样品分别用不同的荧光染料标记,然后两种蛋白质样品在一块胶上进行二维电泳的分离,最后通过荧光扫描技术分析结果。胶染色后可以利用凝胶图像分析系统成像,然后通过分析软件对蛋白质点进行定量分析,并且对感兴趣的蛋白质点进行定位。通过专门的蛋白质点切割系统,可以将蛋白质点所在的胶区域进行精确切割。接着对胶中蛋白质进行酶切消化,酶切后的消化物经脱盐/浓缩处理后就可以通过点样系统将蛋白质点样到特定的材料的表面(MALDI-TOF)。最后这些蛋白质就可以在质谱系统中进行分析,从而得到蛋白质的定性数据;这些数据可以用于构建数据库或和已有的数据库进行比较分析。LCM-二维电泳-质谱的技术路线是典型的一条蛋白质组学研究的技术路线,除此以外,LCM-抗体芯片也是一条重要的蛋白质组学研究的技术路线。即通过LCM技术获得感兴趣的细胞类型,制备细胞蛋白质样品,蛋白质经荧光染料标记后和抗体芯片杂交,从而可以比较两种样品蛋白质表达的异同。Clontech最近开发了一张抗体芯片,可以对378种膜蛋白和胞浆蛋白进行分析。该芯片同时配合了抗体芯片的全部操作过程的重要试剂,包括蛋白质制备试剂,蛋白质的荧光染料标记试剂,标记体系的纯化试剂,杂交试剂等。对于蛋白质相互作用的研究,酵母双杂交和噬菌体展示技术无疑是很好的研究方法。Clontech开发的酵母双杂交系统和NEB公司开发的噬菌体展示技术可供研究者选用。关于蛋白质组的研究,也可以将蛋白质组的部分或全部种类的蛋白质制作成蛋白质芯片,这样的蛋白质芯片可以用于蛋白质相互作用研究,蛋白表达研究和小分子蛋白结合研究。 Science,Vol. 293,Issue 5537,2101-2105,September 14,2001发表了一篇关于酵母蛋白质组芯片的论文。该文主要研究内容为:将酵母的5800个ORF表达成蛋白质并进行纯化点样制作芯片,然后用该芯片筛选钙调素和磷脂分子的相互作用分子。最后有必要指出的是,传统的蛋白质研究注重研究单一蛋白质,而蛋白质组学注重研究参与特定生理或病理状态的所有的蛋白质种类及其与周围环境(分子)的关系。因此蛋白质组学的研究通常是高通量的。适应这个要求,蛋白质组学相关研究工具通常都是高度自动化的系统,通量高而速度快,配合相应分析软件和数据库,研究者可以在最短的时间内处理最多的数据
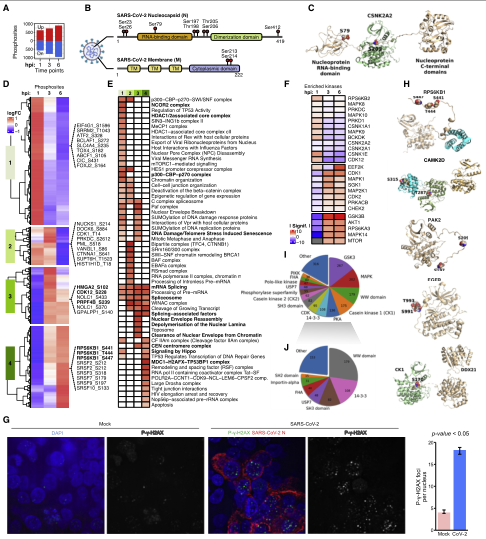
蛋白质组学主要包括哪些分析技术及各自特点.
双向凝胶电泳
双向凝胶电泳的原理是第一向基于蛋白质的等电点不同用等电聚焦分离,第二向则按分子量的不同用SDS-PAGE分离,把复杂蛋白混合物中的蛋白质在二维平面上分开。由于双向电泳技术在蛋白质组与医学研究中所处的重要位置,它可用于蛋白质转录及转录后修饰研究,蛋白质组的比较和蛋白质间的相互作用,细胞分化凋亡研究,致病机制及耐药机制的研究,疗效监测,新药开发,癌症研究,蛋白**检查,小量蛋白纯化,新替代疫苗的研制等许多方面。近年来经过多方面改进已成为研究蛋白质组的最有使用价值的核心方法。
等电聚焦(isoelectricfocusing,IEF)是60年代中期问世的一种利用有pH梯度的介质分离等电点不同的蛋白质的电泳技术。等电聚焦凝胶电泳依据蛋白质分子的静电荷或等电点进行分离,等电聚焦中,蛋白质分子在含有载体两性电解质形成的一个连续而稳定的线性pH梯度中电泳。载体两性电解质是脂肪族多氨基多羧酸,在电场中形成正极为酸性,负极为碱性的连续的pH梯度。蛋白质分子在偏离其等电点的pH条件下带有电荷,因此可以在电场中移动;当蛋白质迁移至其等电点位置时,其静电荷数为零,在电场中不再移动,据此将蛋白质分离。
生物质谱技术是蛋白质组学研究中最重要的鉴定技术,其基本原理是样品分子离子化后,根据不同离子之间的荷质比(M/E)的差异来分离并确定分子量。对于经过双向电泳分离的目标蛋白质用胰蛋白酶酶解(水解Lys或Arg的-C端形成的肽键)成肽段,对这些肽段用质谱进行鉴定与分析。目前常用的质谱包括两种:基质辅助激光解吸电离-飞行时间质谱(MALDI-TOF-MS)和电喷雾质谱(ESI-MS)。
飞行时间质谱
MALDI的电离方式是Karas和Hillenkamp于1988年提出。MALDI的基本原理是将分析物分散在基质分子(尼古丁酸及其同系物)中并形成晶体,当用激光(337nm的氮激光)照射晶体时,基质分子吸收激光能量,样品解吸附,基质-样品之间发生电荷转移使样品分子电离。它从固相标本中产生离子,并在飞行管中测定其分子量,MALDI-TOF-MS一般用于肽质量指纹图谱,非常快速(每次分析只需3~5min),灵敏(达到fmol水平),可以精确测量肽段质量,但是如果在分析前不修饰肽段,MALDI-TOF-MS不能给出肽片段的序列。
电喷雾质谱(ESI-MS)
ESI-MS是利用高电场使质谱进样端的毛细管柱流出的液滴带电,在N2气流的作用下,液滴溶剂蒸发,表面积缩小,表面电荷密度不断增加,直至产生的库仑力与液滴表面张力达到雷利极限,液滴爆裂为带电的子液滴,这一过程不断重复使最终的液滴非常细小呈喷雾状,这时液滴表面的电场非常强大,使分析物离子化并以带单电荷或多电荷的离子形式进入质量分析器。ESI-MS从液相中产生离子,一般说来,肽段的混合物经过液相色谱分离后,经过偶联的与在线连接的离子阱质谱分析,给出肽片段的精确的氨基酸序列,但是分析时间一般较长。目前,许多实验室两种质谱方法连用,获得有意义的蛋白质的肽段序列,设计探针或引物来获得有意义的基因。随着蛋白质组研究的深入,又有多种新型质谱仪出现,主要是在上述质谱仪的基础上进行改进与重新组合
本回答由提问者推荐
什么是蛋白质组学?
这个概念最早是在1995年提出的,它在本质上指的是在大规模水平上研究蛋白质的特征,包括蛋白质的表达水平,翻译后的修饰,蛋白与蛋白相互作用等,由此获得蛋白质水平上的关于疾病发生,细胞代谢等过程的整体而全面的认识。 目前,在蛋白质功能方面的研究是极其缺乏的。大部分通过基因组测序而新发现的基因编码的蛋白质的功能都是未知的,而对那些已知功能的蛋白而言,它们的功能也大多是通过同源基因功能类推等方法推测出来的。有人预测,人类基因组编码的蛋白至少有一半是功能未知的。因此,在未来的几年内,随着至少30种生物的基因组测序工作的完成,人们研究的重点必将转到蛋白质功能方面,而蛋白质组的研究正可以完成这样的目标。在蛋白质组的具体应用方面,蛋白质在疾病中的重要作用使得蛋白质组学在人类疾病的研究中有着极为重要的价值。 疾病的产生可能仅仅是因为基因组中一个碱基对的变化,如β-血红蛋白第六位上的Glu变为Val就导致了镰刀型细胞贫血症的发生。然而,对于大多数疾病来说,其疾病发生机制要复杂的多。因此,对于疾病发生的分子机制的认识就需要一些能够解决这些复杂性的方法来完成。而作为细胞中的活性大分子,蛋白质无疑是与疾病相关的主要分子,蛋白表达水平的改变是与疾病,药物作用或毒素作用直接相关的。因此,基于蛋白质整体水平的蛋白质组学在人类疾病研究中无疑将发挥重要作用。 现在,蛋白质组学在人类疾病中的应用已经在一些疾病如皮肤病,癌症,心脏病中广泛开展了,而这些研究则主要集中在这样几个方面:寻找和疾病相关的单个蛋白,整体研究某种疾病引起的蛋白表达或修饰的变化,利用蛋白质组寻找一些致病微生物引起的疾病的诊断标记和疫苗等。下面,我们就将就蛋白质组学的基本技术和这些领域的应用作一些介绍。 蛋白质组学研究的基本技术 对于蛋白质组学的研究来说,它的最基本的实验手段就是利用双向凝胶电泳(two-dimensional protein electrophoresis, 2DE),在整个 基因组水平上检测蛋白质表达的情况。双向凝胶电泳首先利用等电点聚焦来分离不同等电点的蛋白,再利用SDS-PAGE来分离不同分子量的蛋白,其分辨率是非常高的。微克级的蛋白质就可以被很好的分辨开了,如在微克级水平上,有人从一个蛋白混合物中最多分开了11200种蛋白质,数量是非常可观的。因而,微克级的蛋白的双向凝胶电泳常被用来初步检测表达或修饰有变化的蛋白。然后,同样的蛋白混合物样品可用于毫克级的2DE,这样,电泳图谱上的每一个多肽就可被纯化并进行下一步的分析,如质谱,末端或中间的氨基酸序列分析等。 仅仅进行双向凝胶电泳显然是远远不够的,因为由双向电泳得到的蛋白质表达情况的变化并不能和具体的何种蛋白表达出了变化联系起来。而一些如蛋白质印迹或凝集素亲和印迹等传统技术对于这方面的信息也帮助不大。为了鉴定这些由电泳得来的蛋白,质谱(MS,*ss spectrometry)被广泛应用在蛋白质组学中。对于蛋白质的鉴定,有两种方法用的最为广泛,即MALDI-MS ( *trix-assisted laser desorption ionization)和ESI-MS (electrospray ionization)。这两种方法各有自己的 适用范围,通常前者对于分析高分子量的蛋白更有效,而后者对于蛋 白的检测灵敏度更高,常可达到飞克级水平以下。质谱可以用于蛋白质分析主要是因为它可以提供特定蛋白的不同方面的结构信息,如它可直接测定蛋白或多肽的分子量信息,也可用来获得一些蛋白质序列信息等。同时,质谱也可通过多肽片段分子量的改变来得到一些关于糖型,磷酸化和其它翻译后修饰的数据。因此,质谱对于蛋白质的鉴定是非常重要的,而它的进展也无疑会大大促进蛋白质组学的研究进展。 单个的疾病相关蛋白的寻找 在疾病发生过程中,由于和疾病相关的遗传信息的变化常常会导致蛋白的种类和数量发生变化,而这些变化是可以被可以被高解析度的双向凝胶电泳所检测到的,这就是利用蛋白质组学寻找和鉴定疾病相关蛋白的依据。 结肠癌的产生是一个包含了多个基因突变的多步过程,这其中包括抑癌基因的功能丧失,癌基因的活化等。然而,肿瘤发生的具体机制仍不清楚。对于这样一种涉及多种蛋白的疾病,人们已经开始利用蛋白质组学来分
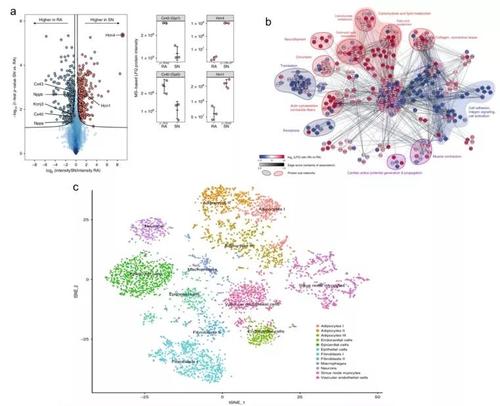
什么是蛋白质组学?在技术上有何特点?
蛋白质组学二楼解释过了。技术上面,核心的是质谱技术,大致就是将一个纯蛋白质用胰酶消化之后,得到多肽片断根据其在电场中的偏转和位移确定其分子量与所带电荷,再综合所有多肽片断的特性与数据库中已知蛋白质进行对比,能对上的,就能够确认蛋白质身份。如此再检测过某个样本中的所有蛋白质之后,能够得到这个样本蛋白质组的详细信息。当然在使用质谱分析之前还有将样本中不同蛋白质进行分离的关键步骤,我听过常用的是二维电泳。一个细胞、组织、生物体基因组表达的全部蛋白质成为蛋白质组。而研究蛋白质组的学问成为蛋白质组学。这是一门庞大的学科系统!蛋白质组学二楼解释过了。技术上面,核心的是质谱技术,大致就是将一个纯蛋白质用胰酶消化之后,得到多肽片断根据其在电场中的偏转和位移确定其分子量与所带电荷,再综合所有多肽片断的特性与数据库中已知蛋白质进行对比,能对上的,就能够确认蛋白质身份。如此再检测过某个样本中的所有蛋白质之后,能够得到这个样本蛋白质组的详细信息。当然在使用质谱分析之前还有将样本中不同蛋白质进行分离的关键步骤,我听过常用的是二维电泳。 ……………… 详细资料请参考:on


